第32周-食道腺癌的類器官
文章亮點
作者成功培養了EAC(食道癌的一種)的organoid ,證明了organoid可以保留腫瘤患者的原位癌
- morphology, genomic, and transcriptomic landscape
- point mutations, copy number alterations, and mutational signatures
提供了非常有意義的a pre-clinical tool
食道癌背景知識
食道癌,跟其它癌症一樣,區分為腺癌 (adenocarcinoma)/ 鱗癌 (squamous cell carcinoma)或其他形態,也就是ESCC和EAC
esophageal squamous cell carcinoma (ESCC)
esophageal adenocarcinoma (EAC)
EAC西方人為主
五年生存率低於15%
前期工作
NGS組學技術已經廣泛應用於該癌症,包括:
- Alexandrov, L. B. et al. Signatures of mutational processes in human cancer. Nature 500, 415–421 (2013).
- Weaver, J. M. J. et al. Ordering of mutations in preinvasive disease stages of esophageal carcinogenesis.Nat. Genet. 46, 837–843 (2014).
- Dulak, A. M. et al. Exome and whole-genome sequencing of esophageal adenocarcinoma identifies recurrent driver events and mutational complexity. Nat. Genet. 45, 478–U437 (2013).
- Nones, K. et al. Genomic catastrophes frequently arise in esophageal adenocarcinoma and drive tumorigenesis. Nat. Commun.5, 5224 (2014).
- Cancer Genome Atlas Research, N. et al. Integrated genomic characterization of oesophageal carcinoma. Nature 541, 169–175 (2017).
- Secrier, M. & Li, X. et al. Mutational signatures in esophageal adenocarcinoma define etiologically distinct subgroups with therapeutic relevance. Nat. Genet. 42, 1131–1141 (2016).
其中2016的. Nat. Genet. 文章是作者做的,使用全基因組測序手段量化了接近100個EAC患者的基因組特性。
而且說明了EAC的細胞系表現不好,急需其它模型,比如最近大放異彩的類器官。
所以作者開始這個研究計劃:
類器官的培養
成功率尚可,達到 31% (10 of 32 samples), 跟其它惡性癌症相當。
那些培養失敗的原因包括:
- lack of growth from culture initiation (n = 11 cultures),
- infection (n = 5)
- fibroblast overgrowth (n = 4)
- arrested growth (n = 2)
摸索這個培養條件並非易事。
培養類器官成功的病人資訊如下:

WGS和RNA-seq測序
資料都在European Genome-phenome Archive (EGA) under accession EGAD00001004007. 需要申請才能下載。
資料分析比較常規,也就是一些軟體的流程連線,值得注意的是作者並沒有選擇GATK的mutect2來找somatic的SNVs,而是採用了strelka,引數如下:
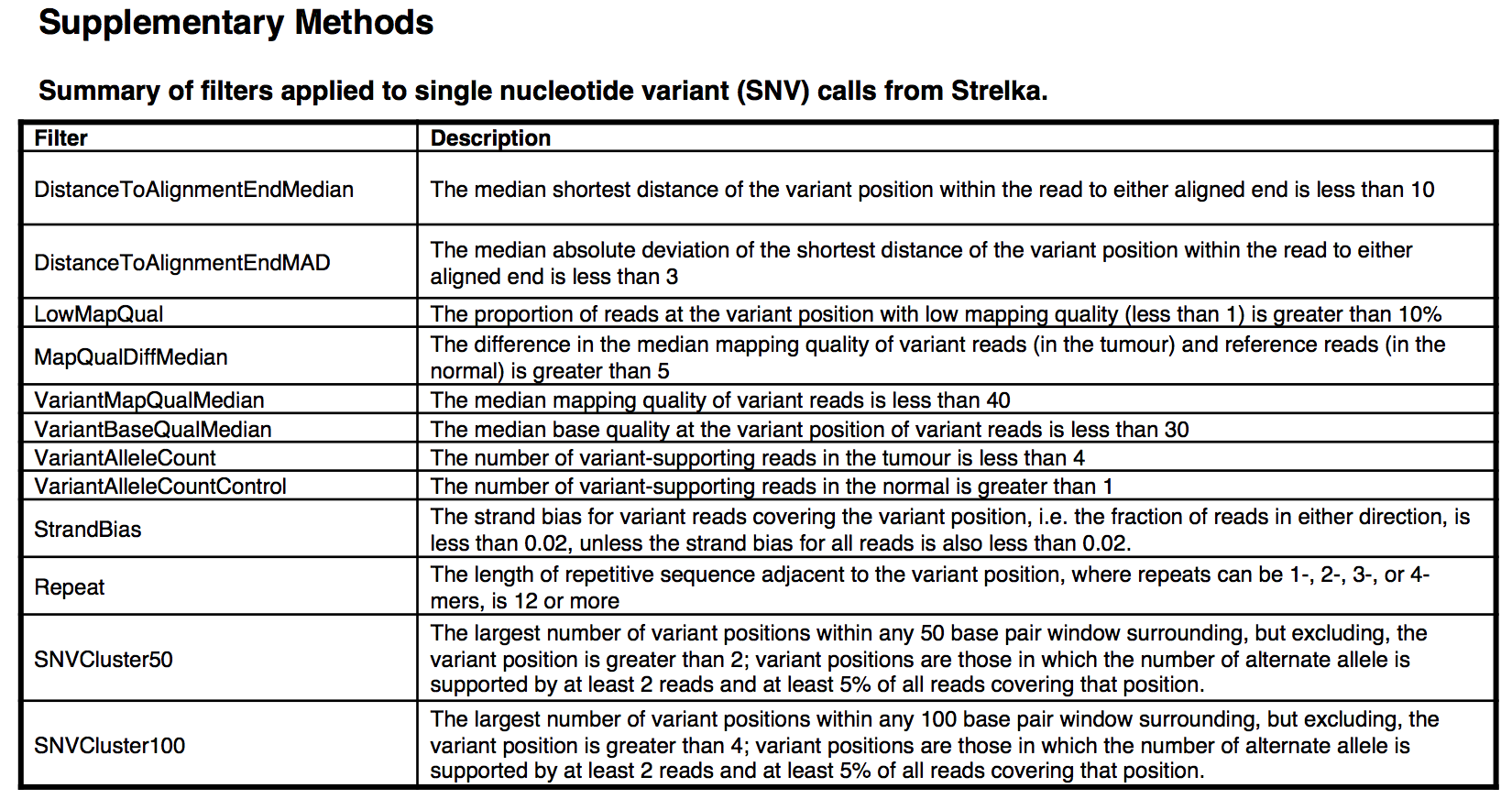
基於RNA-seq測序轉錄組測序主要看錶達量,作者同時也探索了RNA-seq的變異位點。
類器官能重現其原位癌的突變
所有的類器官文章都必須說明這一點,當然要想盡一切辦法來提高同一個病人的原位癌及其對應的類器官測序得到的somatic突變的一致性。
因為作者在2016年了做了n = 129的癌症佇列,其somatic突變結果用MutSigCV找到了可能的driver somatic events,這樣能比較的基因就非常少,這樣能提供突變的一致性。
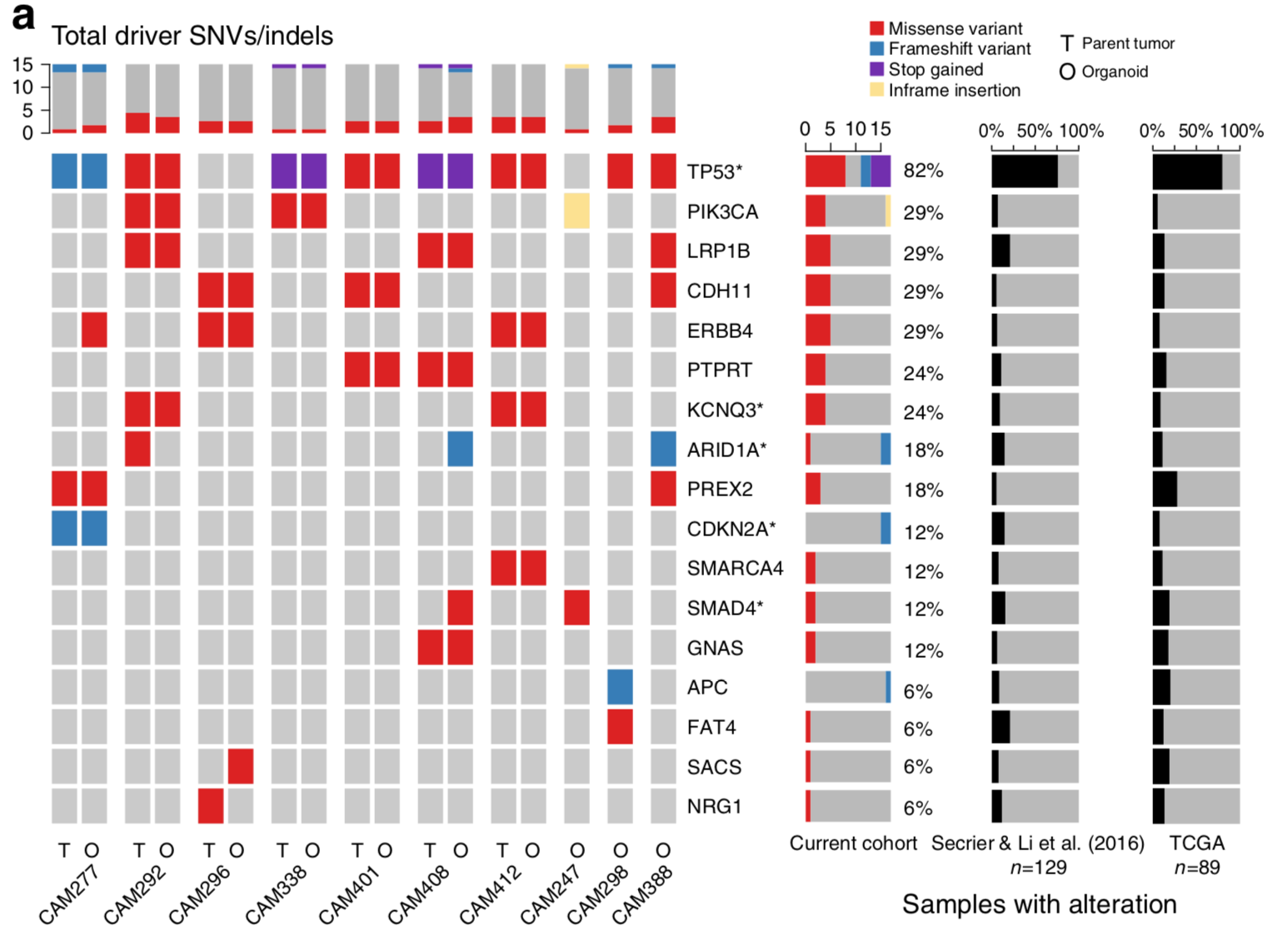
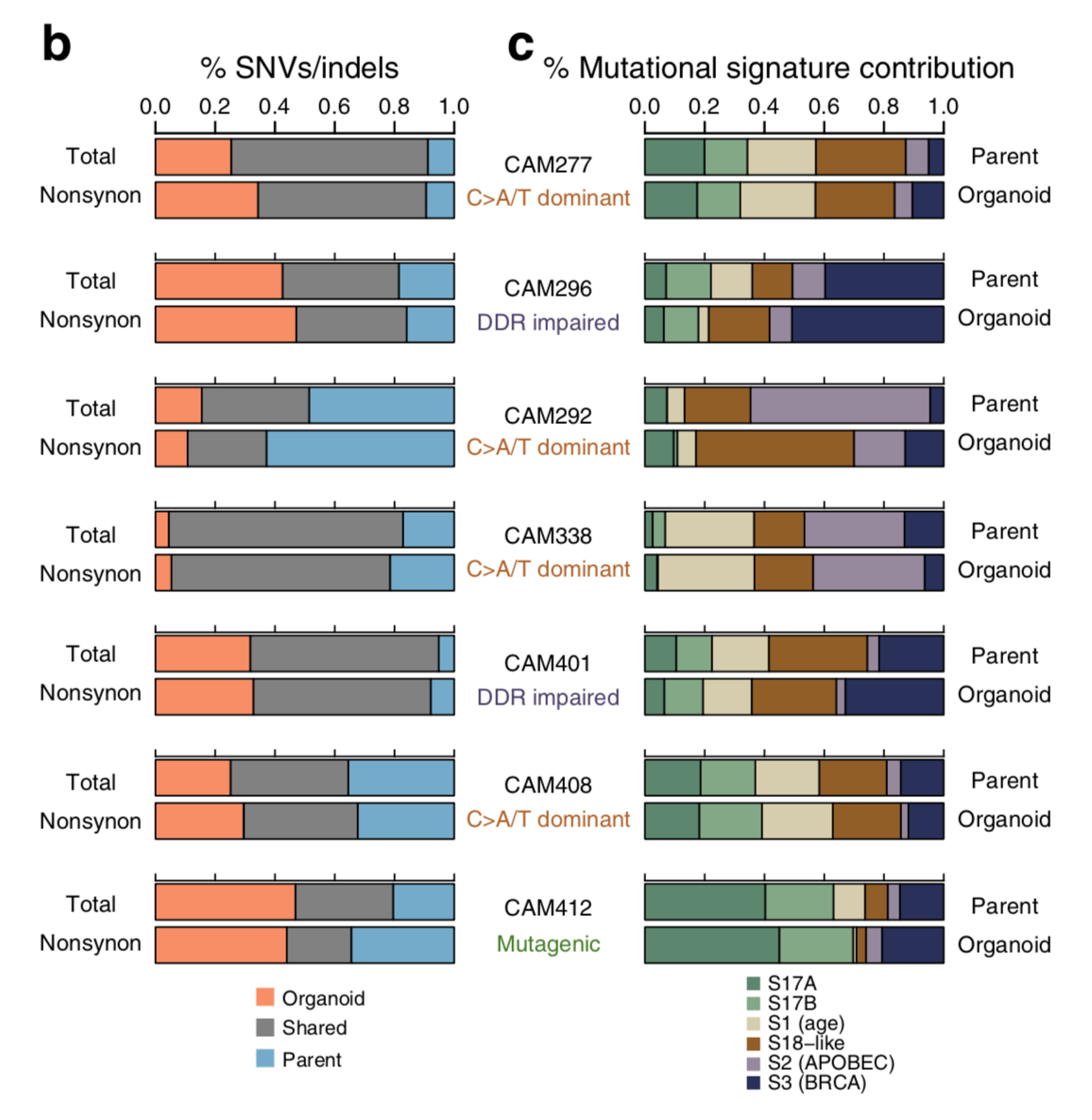
不過這裡作者並不是取巧,因為他們仍然是比較了全部的突變,從SNV,CNV,SV的角度分別比較,都得到了非常好的一致性。
首先看全部的SNVs的一致性,如下:
然後看全部的CNV的一致性,如下:
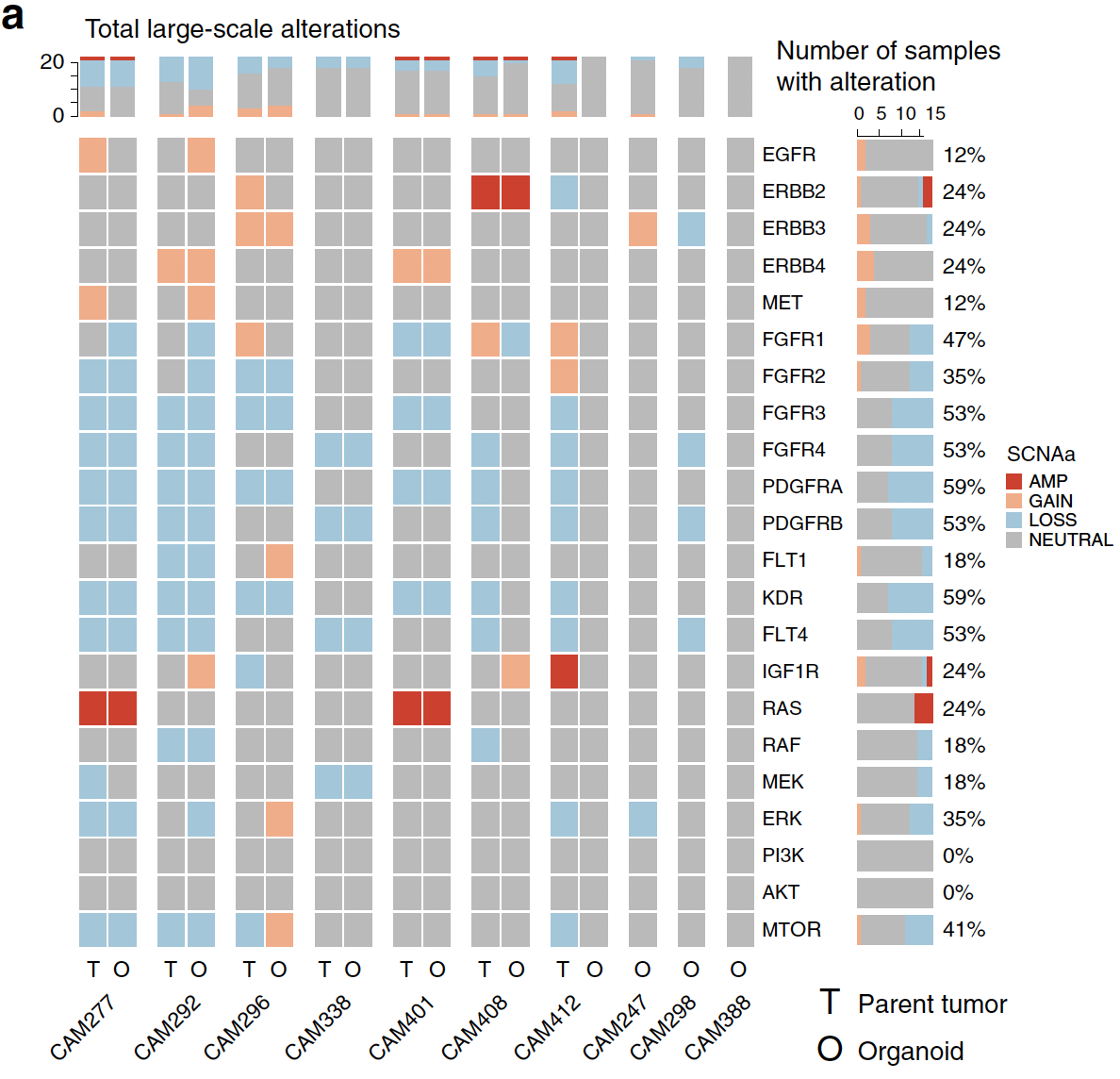
最後看全部的SV的一致性,如下:
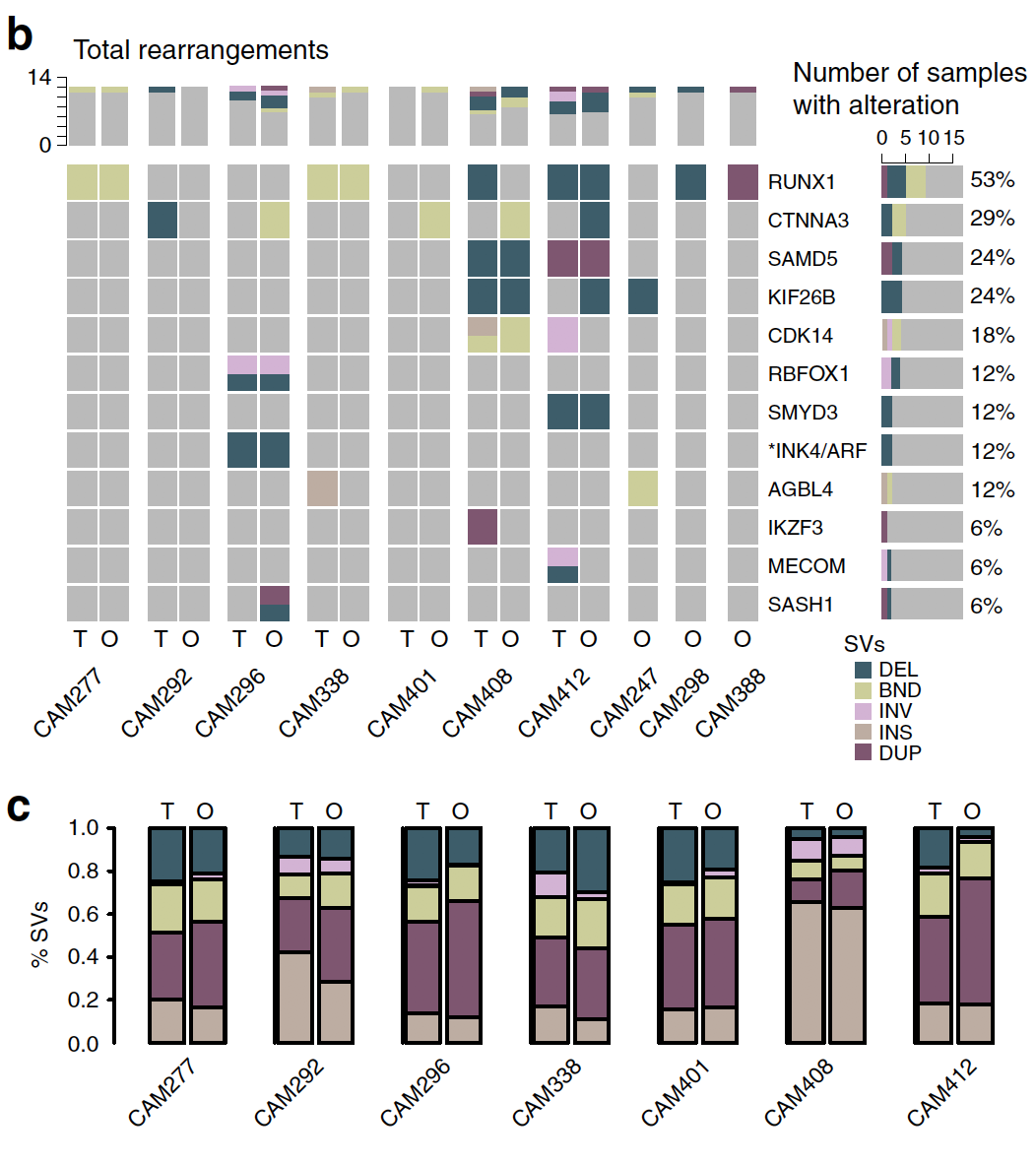
總而言之,organoids比較完美的保留其來源病人的原位癌的分子特性。
還驗證了基於RNA-seq表達量及變異的一致性,也非常好!!!
腫瘤亞克隆
使用Battenberg 演算法對原位癌和類器官都計算copy number aberrations, tumor ploidy, and purity ,而且只探索four tumors (CAM277, CAM296, CAM338, and CAM401).
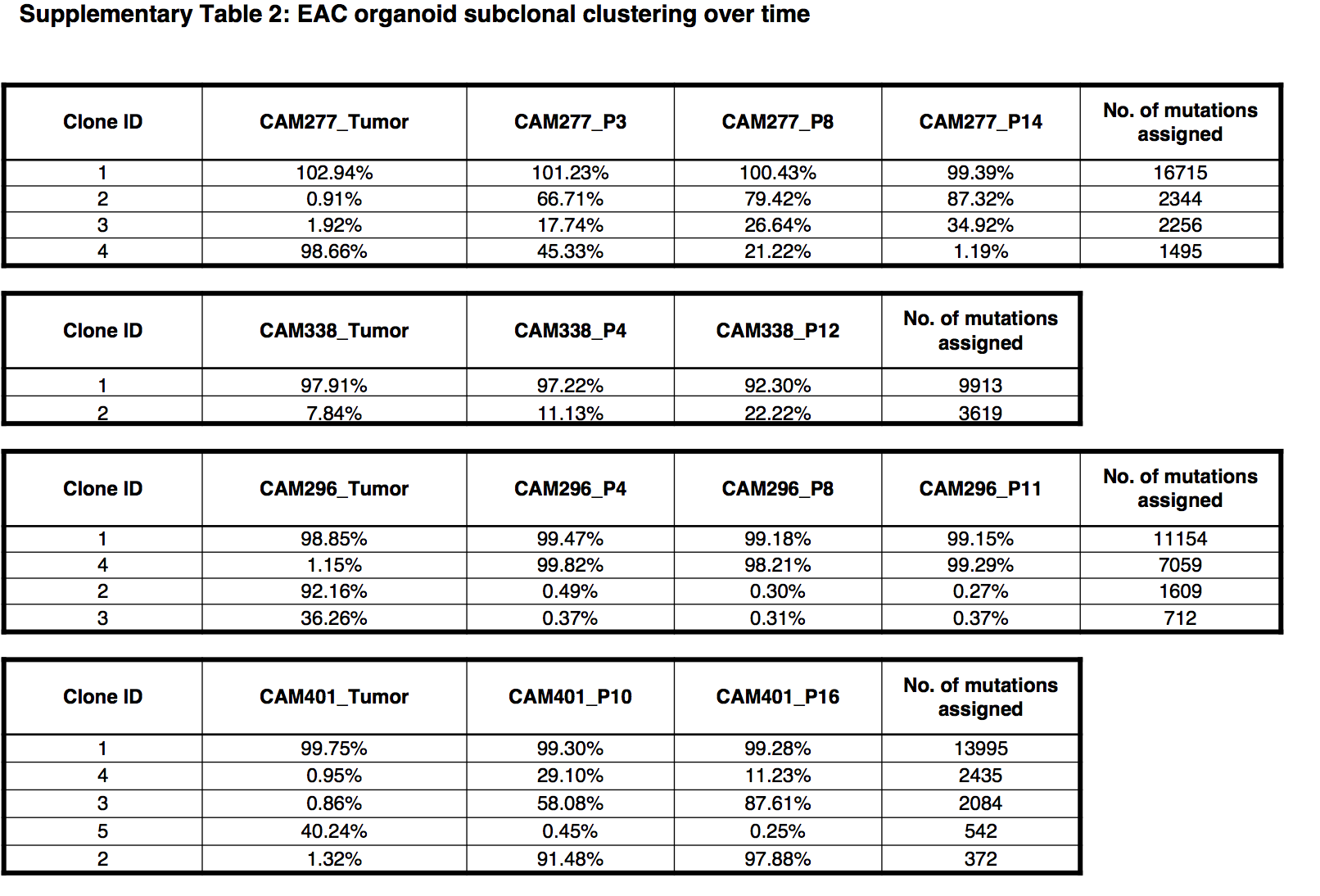
多時間點測序類器官看克隆進化
主圖放2個病人,附件也放兩個病人。
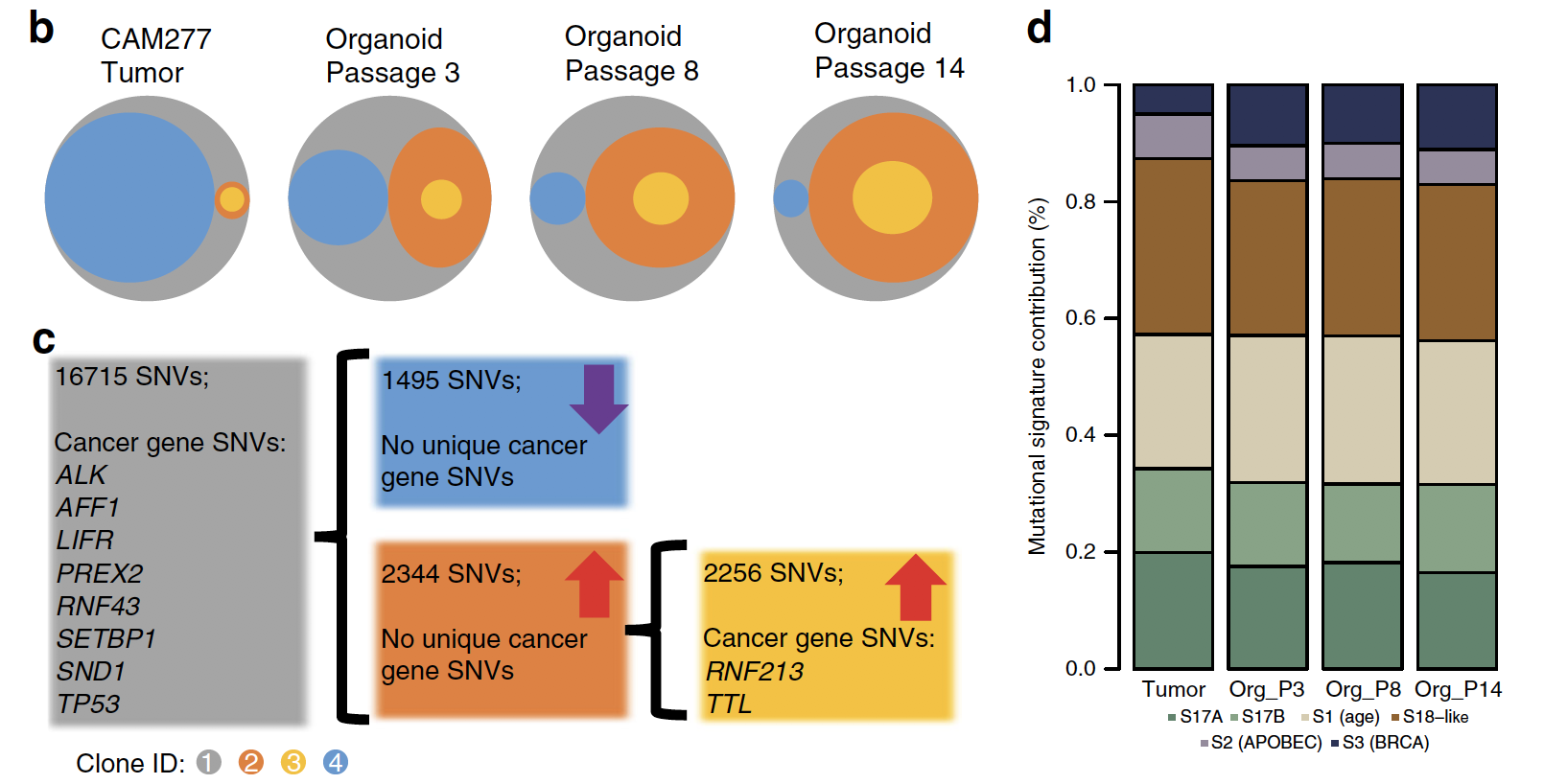
這個病人的類器官培養傳代次數增加,其遺傳特性也變化劇烈。

這個病人的類器官培養傳代次數增加,其遺傳特性很穩定。
藥物處理異質性
作者這裡做了 Drug sensitivity profiling of 24 compounds against nine EAC organoids,然後把藥物反應的IC50結果跟其基因組和轉錄組特性簡單關聯如下;
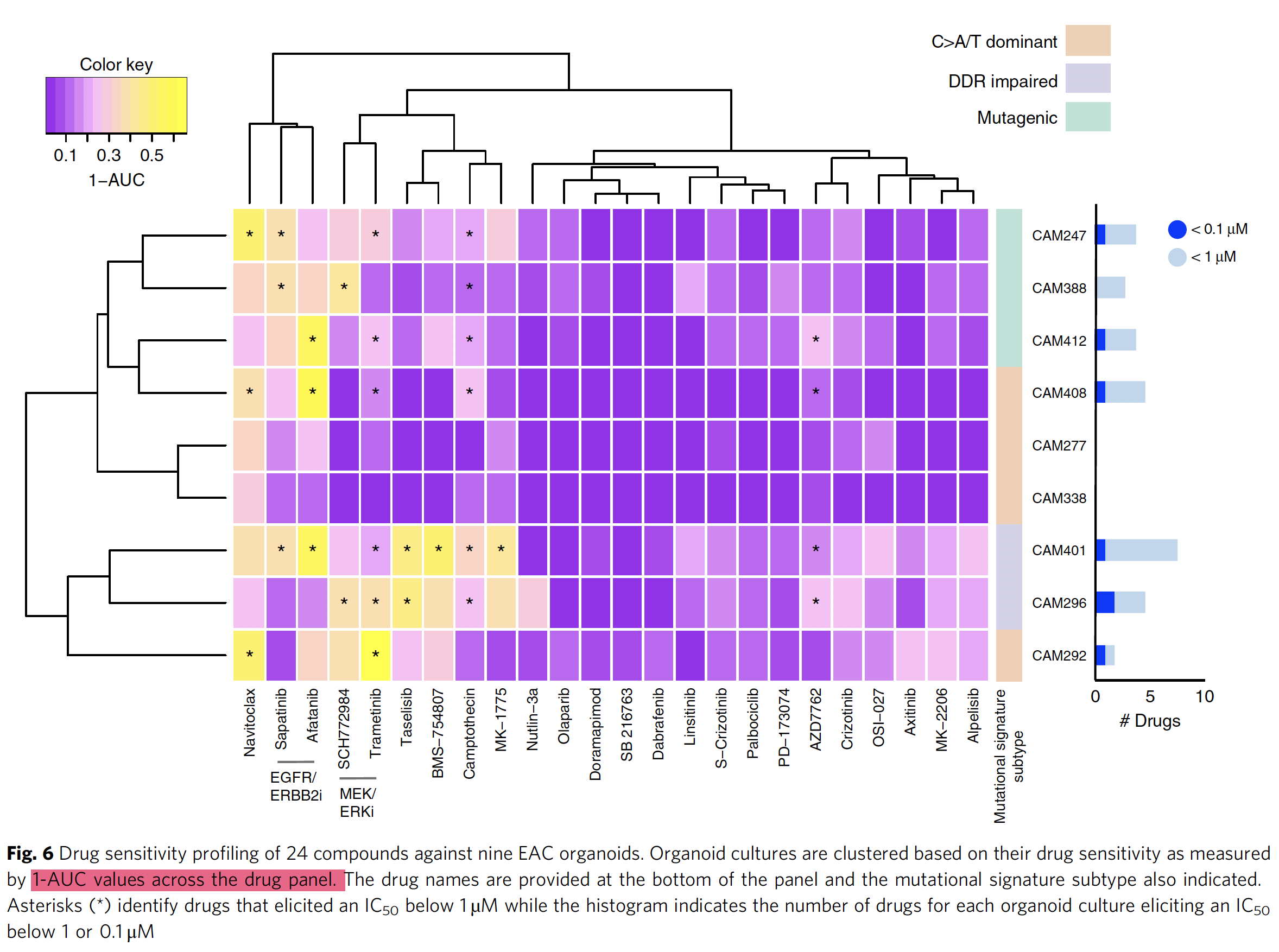
也比較好理解,作者試圖說明某些organoids之所以對某些藥物敏感,是因為它們有某種突變或者某些基因表達譜特性。
